
1.化学键使得100多种元素组成了世界的万物。下列关于化学键的叙述正确的是( )。(D)
A. 离子化合物中一定含共价键,共价化合物中不含离子键
B. 共价化合物中可能含离子键,离子化合物中只含离子键
C. 构成单质分子的粒子一定含有共价键
D. 在氧化钠中,除氧离子和钠离子的静电吸引作用外,还存在电子与电子、原子核与原子核之间的排斥作用
答案解析:共价化合物中一定不含离子键,离子化合物中一定含离子键,可能含共价键,A、B两项错误。构成单质分子的粒子不一定含共价键,如稀有气体,C项错误。氧化钠中含离子键,除氧离子和钠离子的静电吸引作用外,还存在电子与电子、原子核与原子核之间的排斥作用,D项正确。
2.某有机反应的球棍模型如图1所示:
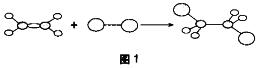 (C)
(C)A. 生成物可能是CH3CH3
B. 生成物可能是CH3CH2OH
C. 该反应属于加成反应
D. 该反应属于取代反应
答案解析:由图可知,因不是与氢气发生加成反应,则生成物不可能是CH3CH3,A项错误;由此可以知道,是与卤素单质发生加成,不是与水发生加成,不能生成乙醇,B项错误;该反应为加成反应,所以C项正确,D项错误。
3.下列说法中正确的是( )。(C)
A. 放热反应都是自发的,吸热反应都是非自发的
B. 自发反应熵一定增大,非自发反应熵一定减小或不变
C. 熵增加且放热的反应一定是自发反应
D. 非自发反应在任何条件下都不能实现
答案解析:反应能自发进行的判断依据是△H-T△S<0,放热反应也可能是非自发的,吸热反应也可能是自发的,A项错误。自发反应熵不一定增大,非自发反应熵不一定减小或不变,△S为正值或负值的反应,并不能判断△H-T△S的大小,B项错误。根据反应能否自发进行的判据,放热日熵增加的反应,△H-T△S一定是小于零的,所以反应一定是自发反应,C项正确。非自发反应在一定的条件下可以实现,D项错误。
4.中国药学家屠呦呦因最早发现并提纯抗疟新药青蒿素而获诺贝尔生理学或医学奖。已知青蒿素的结构式如图2所示。下列有关青蒿素的说法不正确的是( )。
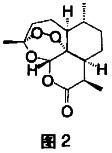 (A)
(A)A. 化学式为C15H20O5
B. 能与NaOH溶液发生反应
C. 与H2O2含有相似结构,具有杀菌作用
D. 可以由低温萃取而得
答案解析:由结构式知青蒿索的化学式为C15H22O5,A项错误。青蒿素中含有酯基,可以发生水解反应,能与NaOH溶液反应,B项正确。青蒿素中含有过氧键,具有氧化性,因此与H2O2含有相似结构,具有杀菌作用,C项正确。过氧基团不稳定,高温易分解,用乙醚为溶剂在低温下从黄花蒿中提取青蒿素是利用其在有机物的溶解性较大,利用了萃取原理,D项正确。
5.电子层相同的三种元素X、Y、Z,它们最高价氧化物对应的水化物的酸性由强到弱的顺序为HXO4>H2YO4>H3ZO4,下列判断错误的是( )。(C)
A. 非金属性强弱的顺序是X>Y>Z
B. 简单气态氢化物稳定性为X>Y>Z
C. 单质与氢气反应由易到难为X<Y<Z
D. 元素原子得电子能力为X>Y>Z
答案解析:同周期元素从左到右,元素的非金属性逐渐增慢,对应的最高价氧化物的水化物的酸性逐渐增强,酸性相对强弱顺序为HXO4>H2YO4>H3ZO4,可知非金属性强弱顺序是X>Y>Z,A项正确。非金属性越强,简单气态氧化物越稳定,由于非金属性X>Y>Z,所以简单气态氧化物的稳定性:X>Y>Z,B项正确。非金属性X>Y>Z,非金属性越强,单质与氢气反应越容易,C项错误。非金属性越强,得电子能力越强,则元素原子得电子能力由强到弱的顺序为X>Y>Z,D项正确。故本题选C。
6.下列各组离子在溶液中能够大量共存的是( )。(A)
A. Na+、Al3+、Cl-、SO42-
B. Cu2+、Cl-、NO3-、OH-
C. Ca2+、Na+、CO32-、NO3-
D. H+、SO42-、NO3、F-
答案解析:A项各离子之间不发生反应,在溶液中能够大量共存;Cu2+,与OH-反应生成Cu(OH)2沉淀,不能大量共存,B项不合题意;Ca2+可与CO32-反应生成CaCO3沉淀,C项不合题意;HF是弱酸,H+和F-不能大量共存,D项不合题意。故本题选A。
7.NA代表阿伏加德罗常数的值,则下列说法正确的是( )。(A)
A. 1L0.1mol/L碳酸钠溶液中,阴离子数目大于0.1NA
B. 标准状况下,11.2L N2和33.6L H2混合在一定条件下充分反应产生的NH3的分子数为2NA
C. 常温常压6g乙酸所含共价键数目为0.7NA
D. 铁和酸反应,放出标准状况下的22.4L气体,转移的电子数必为2NA
答案解析:碳酸根的水解导致溶液中的阴离子的个数增多,故溶液中的阴离子的个数多于0.1NA,A项正确。合成氨的反应为可逆反应,不能进行彻底,故生成的氨气分子个数小于2NA,B项错误。6g乙酸的物质的量为0.1mol,而1mol乙酸中含8mol共价键,故0.1mol乙酸中含共价键数日为0.8NA,C项错误。铁和不同的酸反应,生成的气体的种类不同,可能是氢气、NO2、NO、SO2等,则转移的电子数无法计算,D项错误。故本题选A。
8.下列离子方程式书写正确的是( )。(D)
A. Fe与盐酸反应制H2:2Fe+6H+=2Fe3++3H2[***还有7915个字符未阅读,点击下载文档阅读全文***]





